
L’EMA a émis un avis positif pour modifier la notice/RCP du Librela (bedinvetmab), suite à de nouvelles informations évaluées par le titulaire d’autorisation Zoetis.
Sur base de l’étude de pharmacovigilance, les effets indésirables suivants ont été ajoutés aux informations de produit du Librela :
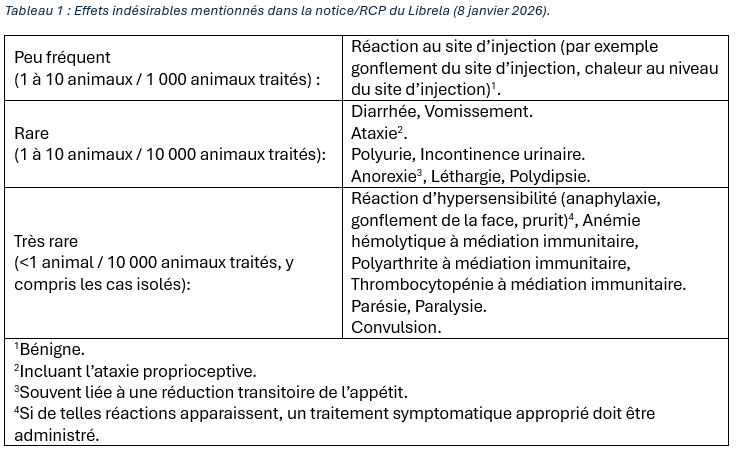
- « diarrhée » et « vomissements » en tant qu’effets indésirables rares (1-10/10.000 animaux traités)
- « polyarthrite à médiation immunitaire », « parésie », « paralysie » et « convulsions » en tant qu’effets indésirables très rares (<1/10.000 animaux traités).
La liste complète des effets indésirables est fournie dans le Tableau 1.
En outre, la notice/RCP mentionne des avertissements concernant le traitement des chiens avec des affections à médiation immunitaire préexistantes, telles que l’anémie hémolytique à médiation immunitaire, la polyarthrite à médiation immunitaire ou la thrombocytopénie à médiation immunitaire, ou des troubles convulsifs préexistants. La notice/RCP indique qu’il « convient d’être prudent » lors du traitement de ces animaux.
Enfin, la durée de conservation du produit passe de 2 à 3 ans.
Source