
Het EMA heeft een positief advies uitgebracht voor wijzigingen in de bijsluiter/SKP van Librela (bedinvetmab) die gebaseerd zijn op nieuwe informatie die door de vergunninghouder Zoetis werd geëvalueerd.
Op basis van het farmacovigilantie-onderzoek worden de volgende bijwerkingen toegevoegd in de productinformatie van Librela:
- ‘diarree’ en ‘braken’ als zeldzame bijwerkingen (1-10/10.000 behandelde dieren)
- ‘immuungemedieerde polyartritis’, ‘parese’, ‘verlamming’ en ‘toevallen’ als zeer zeldzame bijwerkingen (<1/10.000 behandelde dieren)
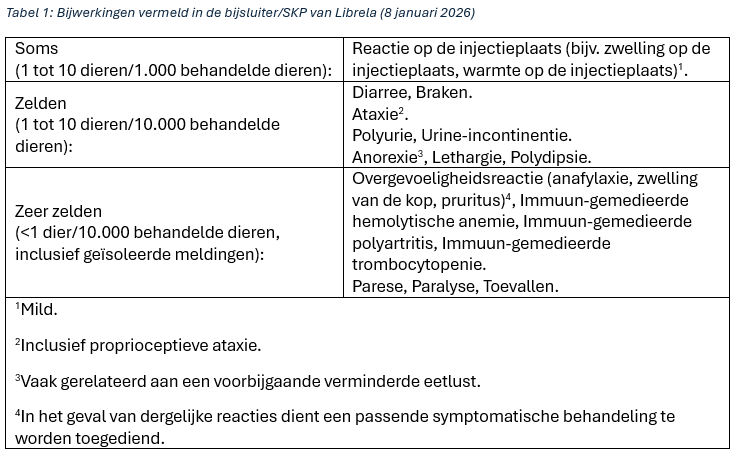
De volledige lijst met bijwerkingen is in Tabel 1 weergegeven.
Daarnaast zijn er waarschuwingen opgenomen voor de behandeling van honden met reeds bestaande immuungemedieerde aandoeningen zoals immuun-gemedieerde hemolytische anemie, immuun-gemedieerde polyartritis en immuun-gemedieerde trombocytopenieen en voor de behandeling van honden met reeds bestaande convulsies. De bijsluiter/SKP vermeldt dat “voorzichtigheid geboden is” bij de behandeling van deze honden.
Tenslotte is de houdbaarheid van het product verlengd van 2 naar 3 jaar.
Bron